Gehirntumore: Onkologe bremst Erwartungen zu neuem Ansatz mit Impfung
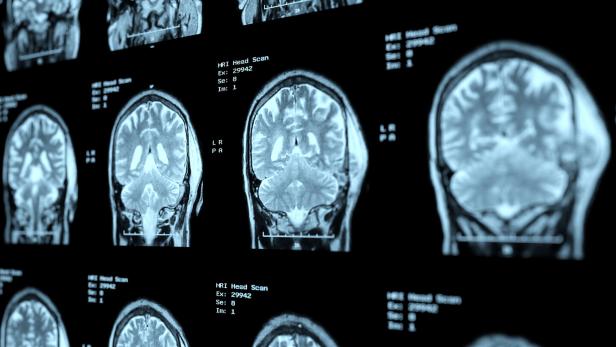
„Der Ansatz ist sehr interessant, aber das Problem ist das Studiendesign.“ Kritisch sieht der Onkologe Matthias Preusser die Ergebnisse einer internationalen Studie mit einer neuen Therapie bei Patienten mit einem Glioblastom, dem häufigsten bösartigen Gehirntumor. Diese sorgte in den vergangenen Tagen international für Aufsehen: Demnach soll ein therapeutischer Impfstoff aus eigenen Abwehrzellen zu einer durchschnittlichen Lebensverlängerung um mehrere Monate im Vergleich zur Standardtherapie führen. Die Autoren bezeichneten die Ergebnisse als erstaunlich.
Doch Preusser, Spezialist für die Therapie von Gehirntumoren und Leiter der Klinischen Abteilung für Onkologie der Uni-Klinik für innere Medizin I von MedUni und AKH Wien, dämpft die Erwartungen. „Anhand dieser Studie können wir nicht sagen, ob diese Therapie wirkt – oder nicht wirkt. Wir wissen es einfach noch nicht.“
Preusser war in den vergangenen Tagen auf dem Kongress der US-amerikanischen neuro-onkologischen Gesellschaft, wo die Studie (veröffentlicht im Fachmagazin Jama Oncology) von der Hauptautorin präsentiert und dann diskutiert wurde.
232 Glioblastom-Patienten an 94 medizinischen Zentren in vier Ländern (USA, Kanada, Großbritannien, Deutschland) erhielten den Impfstoff-Kandidaten DCVax, 99 waren ursprünglich als ungeimpfte Kontrollgruppe geplant.
„Doch während die Studie noch lief, wurde der Studienaufbau geändert und die Ergebnisse der geimpften Patienten wurden mit externen Daten von Ungeimpften in anderen Studien verglichen. Da gibt es aber nicht einmal individuelle Angaben zu einzelnen Patienten, sondern nur Datenpools, wo wichtige individuelle Daten etwa über den jeweiligen Tumor fehlen. Diese Vorgangsweise weicht sehr von den höchsten Standards, die es derzeit gibt, ab. Und deshalb kann man die Ergebnisse der Geimpften und Ungeimpften nicht vergleichen“, sagt Onkologe Preusser.
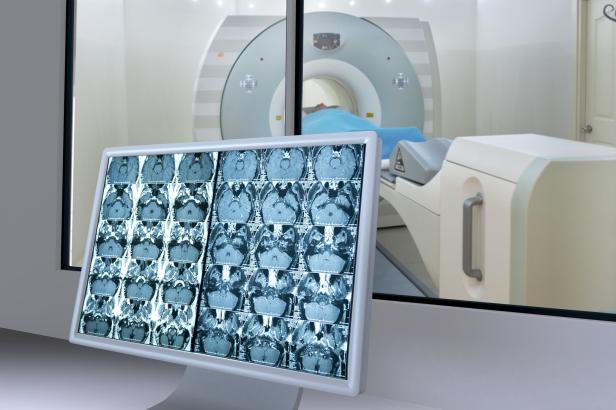
Die ursprüngliche Kontrollgruppe wurde im Laufe der Studie ebenfalls zu einer Behandlungsgruppe. Bei 64 Personen aus der eigentlichen Kontrollgruppe kam es zu einem Wiederauftreten ihres Tumors im Studienzeitraum - daraufhin erhielten auch sie die therapeutische Impfung. Preusser: "So ein Cross-over, ein Wechsel vom Kontroll- zum Therapiepatienten, ist grundsätzlich möglich. Aber auch hier fand dann der Vergleich wieder mit externen, gepoolten Patientendaten statt. Dieses mehrfache Vergleichen von internen und nicht näher definierten externen Daten mindert einfach den wissenschaftlichen Wert dieser Studie enorm."
Fazit: „Auf dem Kongress wurde die Studie wegen ihrer methodischen Schwächen sehr kritisch gesehen. Diese Therapie ist auch noch in keinem Land der Welt zugelassen. Und meiner persönlichen Meinung nach reichen die Ergebnisse nicht aus, um diese Therapie in der Klinik anzuwenden.“ Zudem sei die Firma, die den Impfstoff entwickelt hat, übermäßig stark involviert gewesen: „Man kann deshalb nicht von einer unabhängigen Studie sprechen.“
Enttäuschte Patienten
Deshalb müsse er auch Patientinnen und Patienten enttäuschen, die am Wiener AKH anrufen und große Hoffnungen in diese Therapie setzen: „Derzeit gibt es dafür leider noch keine wissenschaftliche Grundlage. Diese Therapie kann noch nicht angeboten werden, weil es die Datenlage nicht zulässt und auch die Zulassung noch fehlt.“
Der Ansatz der Studie sei theoretisch sehr gut und innovativ: Den Patienten werden eigene Immunzellen entnommen und mit Tumormerkmalen kombiniert. Derart verändert, sollen sie nach der Injektion in den Körper den Tumor aufspüren und besser bekämpfen können. „Eine solche personalisierte Impfung , die auf den jeweiligen individuellen Tumor zugeschnitten ist, ist grundsätzlich eine Behandlungsform, die es wert ist, in gut kontrollierten Studien weiter untersucht zu werden. “ Denn derzeit sei aufgrund der bisherigen Studienergebnisse keine Aussage zur Wirksamkeit möglich.
Preusser betont, dass man in den vergangenen Jahren wissenschaftlich "sehr viel über die Biologie des Glioblastoms" gelernt habe: "Wir verstehen diese Tumorart immer besser, es tut sich sehr viel in der Grundlagenforschung." Zwar seien unmittelbar keine therapeutischen Durchbrüche am Horizont, "aber es gibt Ansätze wie diese therapeutische Impfung und andere zielgerichtete Therapien, wo es noch Forschungsbedarf gibt."

Kommentare