Covid-19: Novavax beantragt Zulassung in Großbritannien
Es ist der erste Antrag auf Zulassung eines sogenannten proteinbasierten Impfstoffs: Heute, Freitag, gab das Biotechnologieunternehmen Novavax den Abschluss seines laufenden Zulassungsantrags bei der britischen Aufsichtsbehörde für Arzneimittel und Gesundheitsprodukte (MHRA) für die Zulassung seines COVID-19-Impfstoffkandidaten bekannt gegeben.
"Der Antrag bringt Novavax der Bereitstellung von Millionen von Dosen des ersten proteinbasierten COVID-19-Impfstoffs deutlich näher. Dieser basiert auf einer bewährten, gut untersuchten Impfstoffplattform, die eine hohe Wirksamkeit gegen mehrere Stämme des Coronavirus aufweist", erklärte Stanley C. Erck, Präsident und Chief Executive Officer von Novavax. "Wir freuen uns auf die Überprüfung durch die MHRA und sind bereit, nach der positiven Entscheidung, von der wir ausgehen, unsere Impfstoffdosen zu liefern. Wir danken den Teilnehmern der klinischen Studien und den Versuchsstandorten im Vereinigten Königreich sowie der UK Vaccines Taskforce für ihre Unterstützung und ihren wichtigen Beitrag zu diesem Programm."
Entwickelt aus genetischer Substanz
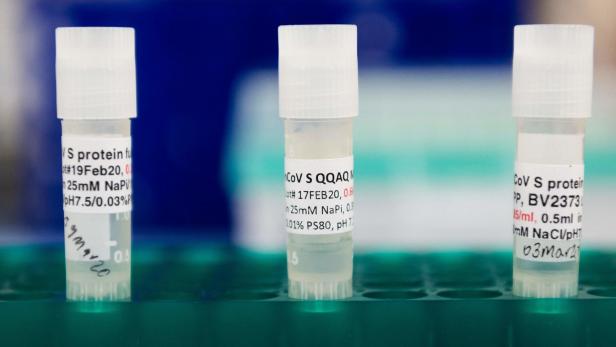
NVX-CoV2373 ist ein proteinbasierter Impfstoffkandidat, der aus der genetischen Sequenz des ersten Stammes von SARS-CoV-2 entwickelt wurde, dem Virus, das die Krankheit Covid-19 verursacht. NVX-CoV2373 wurde mit Hilfe der rekombinanten Nanopartikeltechnologie von Novavax entwickelt, um ein vom Coronavirus-Spike (S)-Protein abgeleitetes Antigen zu erzeugen, und wird mit dem patentierten Saponin-basierten Matrix-M(TM)-Adjuvans von Novavax formuliert, um die Immunantwort zu verstärken und hohe Mengen neutralisierender Antikörper zu stimulieren. NVX-CoV2373 enthält gereinigtes Protein-Antigen und kann sich weder replizieren noch Covid-19 verursachen.
Hoher Schutz
Novavax hat jetzt alle Module eingereicht, die von der MHRA für die behördliche Überprüfung von NVX-CoV2373, dem rekombinanten COVID-19-Impfstoff des Unternehmens auf Nanopartikel-Proteinbasis mit Matrix-M(TM)-Adjuvans, erforderlich sind. Dazu gehören präklinische und klinische Daten sowie Daten zur Chemie, Herstellung und Kontrolle (CMC). Klinische Daten einer zulassungsrelevanten Phase-III-Studie mit 15.000 Freiwilligen in Großbritannien wurden Anfang dieses Jahres an die MHRA übermittelt, in der NVX-CoV2373 eine Wirksamkeit von 96,4 % gegen den ursprünglichen Virusstamm, 86,3 % gegen die Alpha-Variante (B.1.1.7) und insgesamt 89,7 % Wirksamkeit zeigte, ebenso wie ein günstiges Sicherheits- und Verträglichkeitsprofil. Der Antrag enthält außerdem Daten aus PREVENT-19, einer Studie mit 30.000 Teilnehmern in den USA und Mexiko, die einen 100-prozentigen Schutz vor mittelschweren und schweren Erkrankungen sowie eine Gesamtwirksamkeit von 90,4 % gezeigt hat. NVX-CoV2373 war im Allgemeinen gut verträglich und löste eine robuste Antikörperantwort aus.
Novavax geht davon aus, kurz nach der Einreichung in Großbritannien weitere Zulassungsanträge in wichtigen Märkten stellen zu können, unter anderem in Europa, Kanada, Australien, Neuseeland, bei der Weltgesundheitsorganisation und in anderen Märkten auf der ganzen Welt. In den USA geht Novavax davon aus, das Gesamtpaket bis Ende des Jahres bei der FDA einreichen zu können. Das Unternehmen arbeitet weiterhin eng mit Regierungen, Regulierungsbehörden und Nichtregierungsorganisationen (NGOs) zusammen, um weltweit einen gleichberechtigten Zugang zu seinem COVID-19-Impfstoff zu gewährleisten.
Kommentare