Erster Corona-Totimpfstoff: Novavax beantragt EU-Zulassung
Der US-Pharmakonzern Novavax hat für seinen Corona-Impfstoff eine Marktzulassung in der Europäischen Union beantragt. Die in Amsterdam ansässige EU-Arzneimittelbehörde (EMA) teilte am Mittwoch mit, sie habe bereits mit der Prüfung begonnen und werde voraussichtlich in "einigen Wochen" eine Entscheidung bekanntgeben.
Bei dem Vakzin handelt es sich um einen sogenannten Totimpfstoff, der für die Immunisierung also abgetötete Bestandteile des neuartigen Coronavirus enthält.
So funktioniert der Impfstoff
Novavax nennt seinen Impfstoff NVX-CoV2373. Es handelt sich um eine protein-basierten Impfung. Virologin und Impfstoffspezialistin Christina Nicolodi erklärt im KURIER den Unterschied zwischen mRNA und Totimpfung: „Bei den mRNA- und Vektorimpfstoffen erhalten einige Körperzellen die genetische Information, um selbst das Oberflächenprotein (Spike-Protein) des Coronavirus – den eigentlichen Impfstoff – zu produzieren.“
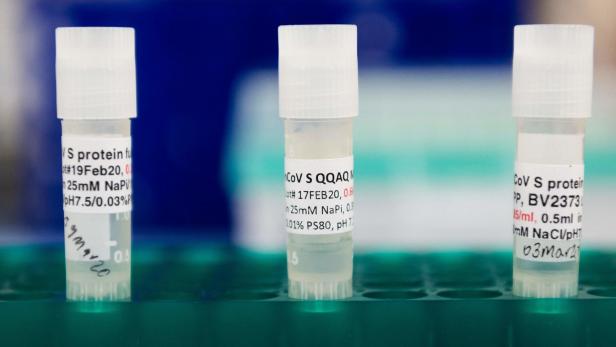
Bei Novavax werden dagegen fertige Proteinpartikel injiziert: Jeweils 14 Partikel werden dann auf einem synthetischen Nanoteilchen montiert – „diese Form ähnelt dann dem Virus und soll so die Immunantwort erhöhen“.
Die Proteinpartikel selbst werden in Insektenzellen vermehrt und von diesen „geerntet“. Dazu werden die Zellen mit einem harmlosen Virus infiziert, das ein Gen für ein modifiziertes Spike-Protein des Coronavirus enthält. Nach der Infektion beginnen die Zellen mit der Produktion des Spike-Proteins. Zusätzlich enthält der Impfstoff noch einen Wirkverstärker aus einem Extrakt des Seifenrindenbaums.
100 Mio. Dosen für EU
Die EU hat bereits eine Vereinbarung über einen Kauf von 100 Millionen Dosen mit Novavax abgeschlossen, für weitere 100 Millionen Dosen gibt es eine Option.
Hoher Schutz
Klinische Daten einer zulassungsrelevanten Phase-III-Studie mit 15.000 Freiwilligen in Großbritannien bescheinigen NVX-CoV2373 eine Wirksamkeit von 96,4 % gegen den ursprünglichen Virusstamm, 86,3 % gegen die Alpha-Variante (B.1.1.7), ebenso wie ein günstiges Sicherheits- und Verträglichkeitsprofil.
Der Antrag enthält außerdem eine Studie mit 30.000 Teilnehmern in den USA und Mexiko, die einen 100-prozentigen Schutz vor mittelschweren und schweren Erkrankungen sowie eine Gesamtwirksamkeit von 90,4 % gezeigt hat. NVX-CoV2373 war im Allgemeinen gut verträglich und löste eine robuste Antikörperantwort aus.
In England läuft Zulassung schon
In Großbritannien läuft die Zulassung schon seit Ende Oktober. Das US-Biotechunternehmen hat bereits weiteren Ländern die Zulassung des Impfstoffs beantragt. Zuletzt am 15. November in Südkorea.
Novavax geht davon aus, weitere Zulassungsanträge in wichtigen Märkten stellen zu können, unter anderem in Kanada, Australien, Neuseeland, bei der Weltgesundheitsorganisation und in anderen Märkten auf der ganzen Welt.
In den USA soll das Gesamtpaket bis Ende des Jahres bei der FDA eingereicht werden. Das Unternehmen arbeitet weiterhin eng mit Regierungen, Regulierungsbehörden und Nichtregierungsorganisationen (NGOs) zusammen, um weltweit einen gleichberechtigten Zugang zu seinem COVID-19-Impfstoff zu gewährleisten.
Kommentare