USA lassen erste Immun-Gentherapie zur Krebsbehandlung zu
In den USA hat mit der Zulassung einer innovativen Gentherapie ein neues Kapitel in der Behandlung von Blutkrebs begonnen. Die nationale Arzneimittelbehörde FDA würdigte die Genehmigung der Kymriah genannten Therapie am Mittwoch als „historisch“. Der Schweizer Pharmakonzern Novartis, der das Patent innehat, gab an, Kymriah habe bei Studien in 83 Prozent der Fälle Wirkung gezeigt.
Kymriah wurde in den USA für bis zu 25 Jahre alte Patienten mit Akuter Lymphatischer Leukämie (ALL) zugelassen. Die Therapie wird soll nur dann eingesetzt werden, wenn es nach der herkömmlichen Behandlung zu einem Rückfall kommt oder der Patient auf diese Behandlungsform nicht anspricht. Die Akute Lymphatische Leukämie macht rund 25 Prozent der Krebserkrankungen im Kindesalter aus. Die Überlebenschancen für Kinder mit den etablierten Therapien liegen zwischen 80 und 90 Prozent.
"Voll personalisiert"
„Es handelt sich um einen neuen Ansatz, der voll personalisiert ist und die eigenen T-Helferzellen des Patienten nutzt“, sagte Novartis-Geschäftsführer Joseph Jimenez.
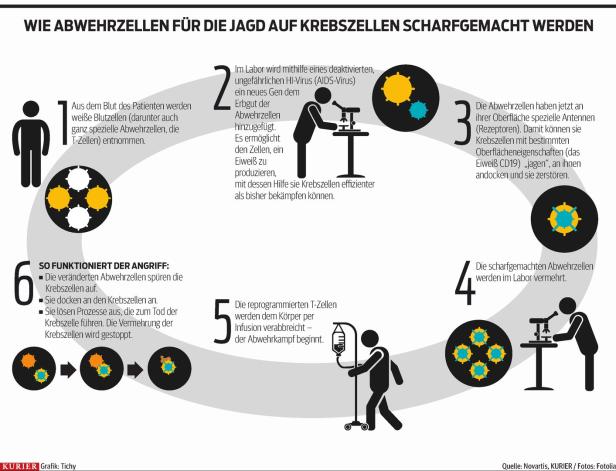
Demnach werden die als T-Zellen bekannten weißen Blutzellen des Erkrankten entnommen und in einem Labor gentechnisch verändert: So sollen sie, zurück im Körper des Patienten, die Krebszellen angreifen.
In den USA soll die Kymriah-Behandlung nach Angaben von Novartis 475.000 Dollar (394.256,31 Euro) kosten. Ein Antrag für die EU-Zulassung der Therapie wird für Ende des Jahres erwartet.
Als Vorreiter der Therapiemethode gilt der Wissenschaftler Carl June von der Universität von Pennsylvania. Der bekannteste Patient ist das inzwischen zwölfjährige Mädchen Emily Whitehead, das im Alter von sechs Jahren behandelt worden war. Sie gilt seitdem als geheilt.

Rückfälle auch bei dieser Therapie
Bereits Ende Jul hatte ein Fachgremium der US-Arzneimittelbehörde FDA die Zulassung empfohlen. Die Basis dafür waren die von Novartis eingereichten Ergebnisse mit der CAR-T-Zelltherapie bei 63 Patienten, die zwischen April 2015 und August 2016 behandelt worden waren. Dabei gab es ein Verschwinden der Erkrankung (Remission) bei 82,5 Prozent (52 Patienten). Elf der 63 Behandelten starben. Laut New York Times gab es bis November 2016 bei elf der zunächst erfolgreich Behandelten Rückfälle. 29 Probanden befanden sich weiterhin in Remission. Elf weitere Probanden erhielten zusätzlich andere Therapien bzw. unterzogen sich einer Stammzelltransplantation.
Kommentare