Impfstoffe - Biontech/Pfizer: Untersuchung auf Langzeiteffekte
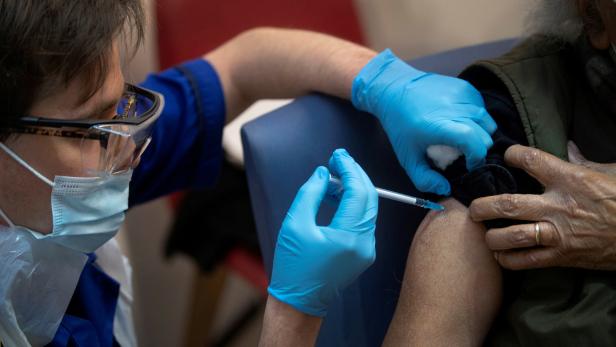
Das zuständige Expertengremium der US-Arzneimittelbehörde FDA (Food and Drug Administration) hat die Zulassung des prophylaktischen Covid-19-Impfstoffs von Biontech/Pfizer empfohlen. Aus den Unterlagen der im Internet übertragenen Sitzung der Fachleute geht hervor, dass jetzt bereits die Untersuchung mögliche Langzeiteffekte der Vakzine läuft. Auf 92 Seiten listeten die Zulassungswerber alle Aspekte der Impfstoffentwicklung auf.
Behörden und auch Skeptiker, die derzeit auf fehlende Langzeitdaten zu der neuen mRNA-Vakzine gegen SARS-CoV-2 verweisen, dürften bald auf Studienergebnisse aus mittel- und längerfristigen Beobachtungen nach Impfung mit BNT162b2 zurückgreifen können. "Pfizer und Biontech beabsichtigen die (für die vorläufige Schnellzulassung; Anm.) Ausschlag gebende Phase-3-Studie mit den Teilnehmern der Vakzin- und der Placebo-Gruppe so lange wie möglich fortzusetzen, um Langzeitdaten zu erhalten und genügend Beobachtungen für eine finale reguläre Zulassung zu erhalten", heißt es in dem offiziellen "Briefing Document" des US-Konzerns Pfizer.
"Wir beabsichtigen in allen Fällen, die Teilnehmer der laufenden Phase-3-Studie bis zum geplanten 24-Monate-Abstand zu beobachten", erklärte Pfizer gegenüber den US-Experten. Darüber hinaus wird die Sicherheit der Vakzine auch weit über die klinischen Studien überwacht werden. "Das Sammeln von Sicherheitsdaten von den Geimpften ist von entscheidender Bedeutung, um das Sicherheitsprofil des Impfstoffes zu verstehen und für das Entdecken von Signalen, welche die Sicherheit im Rahmen der Verwendung im Rahmen der Schnellzulassung betreffen könnten", heißt es in dem Papier.
Deshalb werden auch zusätzlich zur normalen Pharmakovigilanz - also die Meldung von potenziellen Nebenwirkungen durch Ärzte oder anderes Gesundheitspersonal - weitere Studien beginnen. "Zusätzlich (...) werden drei aktive epidemiologische Überwachungsstudien nach der Zulassung (der Vakzine; Anm.) gestartet, um das Auftreten bedeutsamer Sicherheits-relevante Ereignisse in der realen Impfpraxis (real-world; Anm.) zu verfolgen (...)", teilten die Impfstoffentwickler mit.
Gute Verträglichkeit
Insgesamt hat die Wirksamkeitsstudie der mRNA-Vakzine in der Auswertung der Daten von 38.000 Teilnehmern (zur Hälfte Vakzine, zur Hälfte Placebo) offenbar ein gutes Sicherheitsprofil bewiesen. Die Untersuchung hätte gezeigt, dass "30 Mikrogramm sicher und gut verträglich bei Teilnehmer über 16 Jahren waren. Impfreaktionen und Nebenwirkungen waren bei Probanden im höheren Alter (über 56 Jahre) generell milder und seltener als bei Jüngeren (unter 55 Jahre). Die Impfreaktionen waren sowohl bei Erwachsenen als auch bei Jugendlichen (zwölf bis 15 Jahre) in den meisten Fällen mild bis moderat und von kurzer Zeitdauer. Das Nebenwirkungsprofil deutete auf keine Sicherheitsprobleme hin."
Bei der SARS-CoV-2-Vakzine von Biontech/Pfizer handelt es sich um die erste geplante große Anwendung von sogenannten mRNA-Impfstoffen. Die Technik wurde von dem Mainzer Unternehmen Biontech ursprünglich eigentlich für völlig neue Krebsvakzine entwickelt. Im Februar dieses Jahres entschloss man sich bei Biontech zu schnellen Verwendung dieser Technologieplattform für einen Covid-19-Impfstoff. Bei dem Projekt handelt es sich um ein 50:50-Joint Venture des deutschen Unternehmens mit Pfizer als Parnter. mRNA-Krebsvakzine werden mit dem Schweizer Pharmakonzern Roche entwickelt.
"Den Unterschied macht eine neue Herstellungstechnologie. Es ist die Übertragung der in einer mRNA (messenger RNA) codierten genetischen Information eines Impfantigens in Antigen-präsentierende Zellen (Dendritische Zellen; DCs). Die Aufnahme der mRNA führt zu einer Synthese der Impfantigene in den DCs. Die mRNA stimuliert zusätzlich das Immunsystem. Wir geben nicht Eiweiß, sondern mRNA, die für das Eiweiß codiert. Die mRNA braucht auch kein Adjuvans, sondern induziert alle inflammatorischen Zytokine, welche sonst gute Adjuvantien aktivieren", schilderte der aus Österreich stammende Co-Begründer und Hämato-Onkologe Christoph Huber das Prinzip vor kurzem bei den Praevenire Gesundheitstagen im Stift Seitenstetten.
Bei dem SARS-CoV-2-Impfstoff wird über die Impfung die Bauanleitung (mRNA) für den wichtigsten Teil des Spike-Oberflächenproteins (S-Protein) des Virus in den Körper eingebracht. In den Zellen entsteht dann das S-Protein, gegen das eine Immunantwort in Gang kommt. Das Klosterneuburger Biotech-Unternehmen Polymun ist an dem Projekt mit seiner Technologie für die Verpackung der mRNA in Fettstoff-Nanopartikel beteiligt. Erst im Juni dieses Jahres haben BioNTech-Co-Gründer Ugur Sahin und Pfizer-Chef Albert Bourla das Unternehmen besucht. Polymun hat zum Beispiel die Vakzine für die klinischen Untersuchungen produziert und steril abgefüllt.


Kommentare