Revolution in Krebsbehandlung: Medizin-Nobelpreis für Immuntherapie

Die beiden Krebsforscher Tasuku Honjo (links) und James P. Allison.
Den begehrtesten Preis in der Wissenschaft im Bereich Medizin erhalten in diesem Jahr die beiden Krebsforscher James P. Allison und Tasuku Honjo. Beide trugen maßgeblich dazu bei, dass die Immuntherapie als eine wichtige Säule im Kampf gegen Krebs entwickelt werden konnte. Allison forscht derzeit am Cancer Center Houston an der University of Texas, davor arbeitete er in Berkeley an der University of California sowie am Cancer Center New York in den USA. Tasuku Honjo arbeitet an der Kyoto University in Japan. Das Nobelpreis-Komitee hob besonders hervor, dass beide Forscher die Krebstherapie "revolutioniert" und einen "Meilenstein im Kampf gegen Krebs" gesetzt hätten.
Checkpoint-Blockade
Den beiden Preisträgern gelang es, das eigene Immunsystem zu nutzen, um Krebszellen anzugreifen. Sie konnten diese Erkenntnisse auch in die klinische Praxis umsetzen. Zunächst in Experimenten mit Mäusen mit metastasiertem Hautkrebs, dann auch beim Menschen.
Die moderne Immuntherapie beruht auf der sogenannten Checkpoint-Blockade. Mit monoklonalen Antikörpern gegen Oberflächenmerkmale von Tumor- oder Immunzellen (CTLA-4, PD-1 oder PD-L1) wird die Immunabwehr von Patienten wieder gegen die bösartigen Zellen aktiviert. Damit kann bei manchen Krebserkrankungen bei etwa 20 Prozent der Behandelten eine langfristige Kontrolle des Leidens erreicht werden.
„Vor 2010 hat es gegen ein Melanom (schwarzer Hautkrebs, Anm.), das bereits Metastasen gebildet hat, praktisch nichts gegeben“, erinnert sich Hauptkrebsspezialist Hubert Pehamberger, langjähriger Leiter der Hautklinik von AKH Wien/MedUni Wien und jetzt ärztlicher Direktor des Rudolfinerhauses in Wien. „Es gab zwar Chemotherapien, aber der Anteil der Patienten, die darauf ansprachen, lag bei nur rund zehn Prozent. Ein Melanom mit Metastasen bedeutete damals ein Todesurteil. 2010 war das metastasierende Melanom der erste Tumor, bei dem die neue Immuntherapie funktioniert hat. Das war ein gewaltiger Durchbruch. Ich freue mich, dass dieser Ansatz jetzt auch mit dem Nobelpreis gewürdigt wurde.“
Krebsexperte Christoph Zielinski: "Sensationell"
Vom KURIER mit den heurigen Preisträgern konfrontiert, lautete die erste spontane Reaktion des Krebsspezialisten Univ.-Prof. Dr. Christoph Zielinski "sensationell. Der Preis hätten ihnen schon im letzten Jahr gebührt. Das freut mich sehr."
KURIER: Welche Bedeutung haben die Entdeckungen der beiden Preisträger?
Christoph Zielinski: Es handelt sich um den wichtigsten Schritt in der Behandlung onkologischer Krankheiten der vergangenen Jahre. Hier muss man wirklich von einem sensationellen Meilenstein sprechen, der Preis für die beiden ist hochverdient.
Was ist das Besondere an der Immuntherapie?
Es ist ein völlig neues Konzept zur Behandlung onkologischer Erkrankungen. Der Durchbruch kam durch ein Umdenken im Ansatz: Lange Zeit hat man geglaubt, man muss das Immunsystem im Kampf gegen Krebs stärken. Aber ich muss die Bremsen des Immunsystems lösen – also die Paralyse paralysieren, die Lähmung lähmen. Tumorzellen können die Immunzellen in ihrer Wirkung unterdrücken, da können sie das Immunsystem noch so gut gestärkt haben, wird es von Tumorzellen unterdrückt in seiner Wirkung.
Wie funktioniert das genau?
Die Unterdrückung des Immunsystems passiert durch eine Brückenbildung zwischen der Tumorzelle und den weißen Blutkörperchen (den Abwehrzellen, Anm.) Die neuen Antikörper sind gegen diese Brücke gerichtet und heben diese Brückenbildung auf. Damit wird diese Paralyse, diese Lähmung, die der Tumor auf das Immunsystem ausübt, paralysiert.
Wann hat diese Entwicklung begonnen?
Es hat mit dem Melanom 2010 begonnen. Da hat man gesehen, dass der Antikörper Ipilimumab besser ist als jede Art von Chemotherapie. Bei zwei Drittel aller Patienten mit metastasiertem Melanom sieht man auch zwei Jahre nach Therapiebeginn kein Fortschreiten der Erkrankung, das ist schon bemerkenswert. Die Erkrankung ist also unter Kontrolle gekommen, mit Metastasen. Und bei nicht-kleinzelligem Lungenkarzinom (rund 80% aller Lungenkrebserkrankungen) leben unter gewissen Kriterien nach fünf Jahren noch mehr als 40 Prozent der Patienten.
Was ist der nächste Schritt?
Der nächste Schritt ist jetzt, Immuntherapeutika mit Chemotherapie zu kombinieren – das bringt noch bessere Daten. In Zukunft wird es viel mehr Kombinationstherapien geben. Nach Haut- und Lungenkrebs haben wir mittlerweile eine Lawine an Zulassungen gegen verschiedenste onkologische Erkrankungen.
Was passiert bei der Immuntherapie genau?
Bei der Immuntherapie geht es darum, die "Tarnkappe", unter der sich Tumoren vor dem Zugriff von Immunzellen schützen, zu entfernen, die Bremsen zu lösen: Möglich machen dies neue Antikörper, mit deren Hilfe die Unterdrückung des Immunsystems durch den Tumor rückgängig gemacht wird. "Hier wird oft fälschlich behauptet, dass das Immunsystem gestärkt werden soll", sagte kürzlich der Krebsspezialist Christoph Zielinski: "Das stimmt nicht. Das stärkste Immunsystem kann einen Tumor nicht besiegen, wenn dieser das Immunsystem lähmt." Die Immuntherapien heben diese Lähmung auf: "Die weißen Blutkörperchen in und rund um den Tumor können ihn so attackieren und zunehmend ausschalten.“
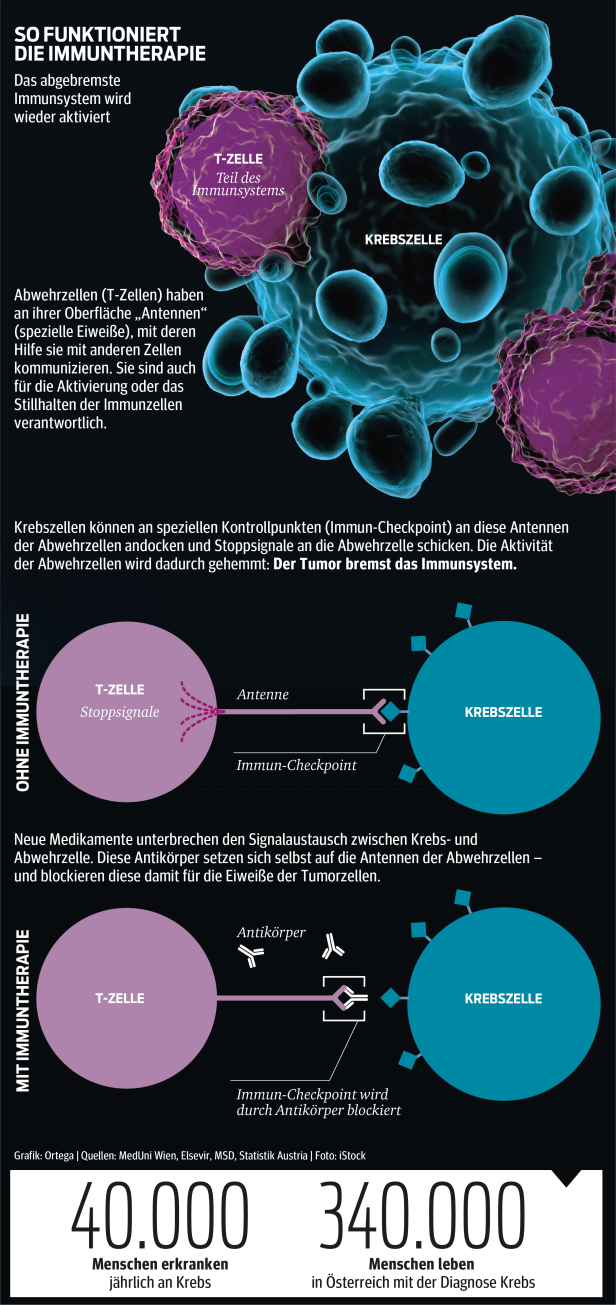
Große Erfolge mit einer solchen Immuntherapie gibt es beim schwarzen Hautkrebs: Die Lebenserwartung von Patienten mit fortgeschrittener Erkrankung konnte durch eine Kombination von zwei Antikörpern deutlich verlängert werden.
Lebenserwartung gestiegen
Patienten mit metastasiertem schwarzen Hautkrebs hatten noch vor wenigen Jahren eine Lebenserwartung von nur vier bis fünf Monaten. Heute leben drei Jahre nach Diagnose der Metastasen zwei Drittel der Patienten, und das mit relativ guter Lebensqualität. Innerhalb der vergangenen 25 Jahre ist in den USA die Krebs-Todesrate um 21 Prozent zurückgegangen, in Europa ist die Entwicklung vergleichbar.
Erste Erfolge gab es in letzter Zeit auch beim Lungenkrebs. "Wir wissen heute, dass ein Drittel der Lungenkrebspatienten von der Immuntherapie allein" profitiert. Ziel ist, jene Patienten, die das nicht tun, für die Immuntherapie zugänglich zu machen, indem man Chemo- oder Strahlentherapie mit Immuntherapie kombiniert. So können Tumore, die nicht auf Immuntherapie sensibel sind, sensibel gemacht werden,“ sagte kürzlich der Lungenkrebsspezialist Maximilian Hochmair.
Preisträger James P. Allison über seinen Durchbruch:
Den von vielen Wissenschaftern ersehnten Anruf machte Thomas Perlmann, der Generalsekretär des Nobelpreis-Kommittees.
Medizin-Nobelpreis: Die Preisträger seit 2007
Der Medizin-Nobelpreis wird seit 1901 verliehen. Die erste Auszeichnung ging damals an den deutschen Bakteriologen Emil Adolf von Behring für die Entdeckung der Serumtherapie gegen Diphtherie. Die Preisträger der vergangenen Jahre waren:
2017: Die US-Forscher Jeffrey Hall, Michael Rosbash und Michael Young für die Erforschung der biologischen "Inneren Uhr" von Organismen.
2016: Der Japaner Yoshinori Ohsumi, der das lebenswichtige Recycling-System für Proteine in Zellen entschlüsselt hat.
2015: Die Chinesin Youyou Tu, die den Malaria-Wirkstoff Artemisinin entdeckt hat. Sie teilte sich den Preis mit dem gebürtigen Iren William C. Campbell und dem Japaner Satoshi Omura, die an der Bekämpfung weiterer Parasiten gearbeitet hatten.
2014: Das norwegische Ehepaar May-Britt und Edvard Moser sowie John O'Keefe ( USA/Großbritannien) für die Entdeckung grundlegender Strukturen des Orientierungssinns des Menschen,
2013: Thomas Südhof (gebürtig in Deutschland) sowie James Rothman (USA) und Randy Schekman (USA) für die Entdeckung von wesentlichen Transportmechanismen in Zellen.
2012: Der Brite John Gurdon und der Japaner Shinya Yamanaka für die Rückprogrammierung erwachsener Körperzellen in den Embryonalzellen.
2011: Bruce Beutler (USA) und Jules Hoffmann (Frankreich) für Arbeiten zur Alarmierung des angeborenen Abwehrsystems. Ralph Steinman aus Kanada entdeckte Zellen, die das erworbene Immunsystem aktivieren. Er war kurz vor der Verkündung gestorben und bekam den Preis posthum.
2010: Der Brite Robert Edwards für die Entwicklung der Reagenzglas-Befruchtung.
2009: Elizabeth Blackburn, Carol Greider und Jack Szostak (alle USA) für die Erforschung der Zellalterung.
2008: Harald zur Hausen (Deutschland) für die Entdeckung der Papilloma-Viren, die Gebärmutterhalskrebs auslösen, sowie die Franzosen Francoise Barre-Sinoussi und Luc Montagnier für die Entdeckung des Aidserregers HIV.
Der Nobelpreis-Fahrplan
Mit Bekanntgabe des Preisträgers für Medizin startet die traditionelle Nobelpreiswoche: Nach den Preisträgern für Medizin und Physiologie verkündet die Königlich-Schwedische Akademie der Wissenschaften die Preisträger in Physik und Chemie. Am Dienstag werden um 11.45 Uhr in Stockholm die Preisträger für Physik und am Mittwoch um 11.45 Uhr jene für Chemie bekannt gegeben. Danach gibt es einen Ortswechsel: Den Träger des Friedensnobelpreises wählt eine Jury in der norwegischen Hauptstadt Oslo. Dort wird er am Freitag um 11 Uhr auch verkündet. Der Literaturnobelpreis fällt in diesem Jahr nach einem Skandal im Jurygremium aus - der KURIER berichtete.
Am Montag, dem 8. Oktober, folgt um 11.45 Uhr die Bekanntgabe der Preisträger für Wirtschaft. Dieser Preis wurde nicht von Alfred Nobel, sondern nachträglich von der schwedischen Reichsbank gestiftet, wird zumeist aber als Nobelpreis angesehen.
Die eigentliche Verleihung der Nobelpreise findet am 10. Dezember, dem Todestag von Preisstifter Alfred Nobel, statt.
Kommentare