Pfizer/Biontech: 90-prozentige Wirksamkeit bei 5- bis 11-Jährigen
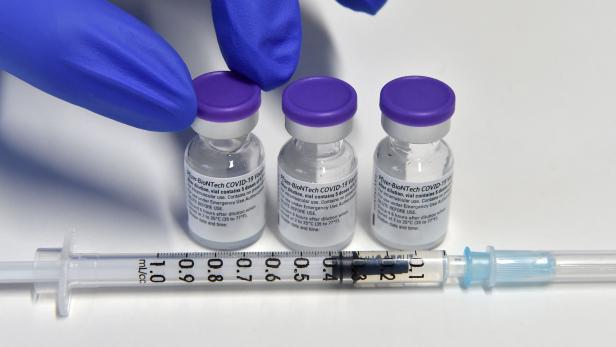
Das Hersteller-Gespann erklärte am Freitag, dass der entwickelte Impfstoff bei Kindern zwischen 5 und 11 Jahren zu 90,7 Prozent wirksam gegen symptomatische Corona-Ansteckungen sei.
Die Meldung kommt unmittelbar vor einem Meeting der US-amerikanischen Food and Drug Administration (FDA), in dem final über eine Zulassung der Vakzine für jüngere Kinder entschieden werden soll. Die Sitzung ist für den 26. Oktober angesetzt.
In der zugrunde liegenden Studie, an der rund 2.000 Kinder teilnahmen, traten in der Gruppe, die den Impfstoff erhielt, drei Covid-19-Fälle auf, in der Placebogruppe dagegen 16 Fälle. Im Rahmen der Studie erhielten doppelt so viele Kinder den Impfstoff wie das Placebo.
Anfang Oktober suchten deutsche Pharma-Unternehmen Biontech und sein US-Partner Pfizer bei der US-Behörde um die Genehmigung des Impfstoffs für Kinder im Alter von fünf bis elf Jahren an. Der Zulassungsantrag enthält eine geplante Verabreichung von zwei Dosen einer 10-Mikrogramm-Dosis. Die beiden Dosen sollen im Abstand von drei Wochen gespritzt werden.
Sollte der Impfstoff zugelassen werden, wäre dies der erste Covid-19-Impfstoff für jüngere Kinder.
Biontech und sein US-Partner Pfizer haben am 15. Oktober auch in Europa eine Zulassung ihres Corona-Impfstoffs für Kinder von fünf bis elf Jahren beantragt. Man habe der EU-Arzneimittelbehörde EMA in Amsterdam die Daten zu den klinischen Untersuchungen übermittelt.
Sicher und wirksam
Ende September hatte das Pharma-Duo eine Studie vorgelegt, die zeigt, dass der Impfstoff in der besagten Altersgruppe gut vertragen wird und eine starke Immunantwort erzeugt.
Es handelte sich um die ersten Ergebnisse aus einer zulassungsrelevanten Studie für einen Covid-19-Impfstoff für Kinder unter zwölf Jahren. In der Studie testeten Biontech und Pfizer eine Dosierung ihres bereits zugelassenen Vakzins von zehn Mikrogramm. Zwei Dosen wurden mit einem Abstand von 21 Tagen verabreicht. Die Impfung für über Zwölfjährige sieht eine Dosierung von 30 Mikrogramm vor.
Die Immunantwort bei Kindern sei bei der niedrigeren Dosierung vergleichbar mit der gewesen, die in einer vorherigen Studie mit 16- bis 25-Jährigen beobachtet wurde, ebenso wie die Nebenwirkungen. An der Untersuchung nahmen 2.268 Kinder im Alter von fünf bis elf Jahren teil.
Für Kinder im Alter von zwölf bis 15 Jahren wurde der Pfizer-Impfstoff in den USA rund einen Monat nach Einreichung des Antrags zugelassen.
Obwohl Kinder weniger anfällig für schwere Verläufe von Covid-19 sind, können sie das Virus an andere – potenziell vulnerable – Personen übertragen.

Kommentare