Zellmutationen beeinflussen Schwere von COVID-19-Verläufen
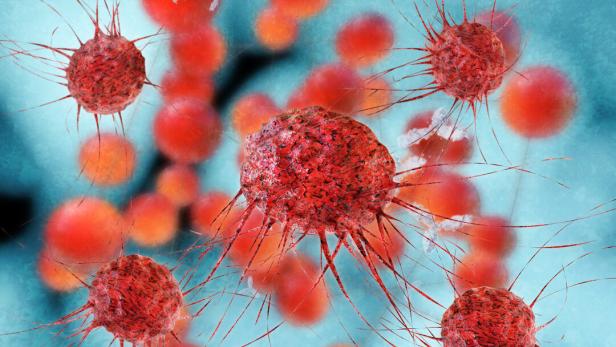
Metastasen entstehen, indem sich Krebszellen vom ursprünglichen Tumor ablösen, mit dem Blut oder mit der Lymphe wandern und sich in anderen Körperteilen wieder ansiedeln und vermehren.
Natürliche Killerzellen (NK-Zellen) spielen bereits zu Beginn einer Infektion eine wichtige Rolle bei der Bekämpfung der Virusvermehrung. NK-Zellen haben spezielle Rezeptoren, die an Antikörper binden, die spezifisch gegen Viren gebildet werden. Wenn die Killerzellen aktiviert wurden, zerstören sie virusinfizierte Zellen und lösen die Ausschüttung von entzündungsfördernden Faktoren aus.
Diese Interaktion zwischen Antikörper und NK-Zell Oberflächenrezeptor wird durch bestimmte genetische Faktoren beeinflusst, die entweder in stark (hoch-affin) oder schwach (niedrig-affin) bindenden genetischen Rezeptorvarianten resultiert. Eine Forschungsgruppe des Zentrums für Virologie der Medizinischen Universität Wien hat nun in Kooperation mit der Klinik Favoriten gezeigt, dass Personen, die aufgrund einer SARS-CoV-2 Infektion mit schwerem Verlauf hospitalisiert werden mussten, signifikant häufiger die hoch-affine Variante des CD16a Rezeptors aufwiesen.
15 Prozent der Bevölkerung betroffen
Sie kommt in etwa 15 Prozent der Bevölkerung vor. Besonders häufig war diese hoch-affine Variante bei Patienten, die mit COVID-19 auf Intensivstationen behandelt werden mussten oder mit COVID-19 verstarben.
Hannes Vietzen: „Bei der Antikörper-abhängigen Aktivierung von NK-Zellen handelt es sich um eine relativ späte Immunantwort. Diese späte Immunantwort scheint nun nicht mehr zur Kontrolle der SARS-CoV-2 Virusvermehrung, sondern durch eine überschießende Immunreaktion zu einer Verschlechterung der COVID-19-Erkrankung beizutragen.“
Bei den Tests handelt es sich um wissenschaftliche Spezialuntersuchungen. Eine routinemäßige Untersuchung in Labors auf diese Parameter ist nicht angedacht, da es derzeit keine auf diese genetische Prädisposition abzielenden therapeutischen und präventiven Möglichkeiten gibt, um das Risiko einer schwer verlaufenden COVID-19 zu verringern. Dabei ist die genetische Prädisposition nur einer von mehreren Faktoren, die die Schwere der Erkrankung beeinflussen.

Kommentare